Capricor控訴Nippon Shinyaku違約求撤回美國分銷協議,投資人憂商業化受阻。
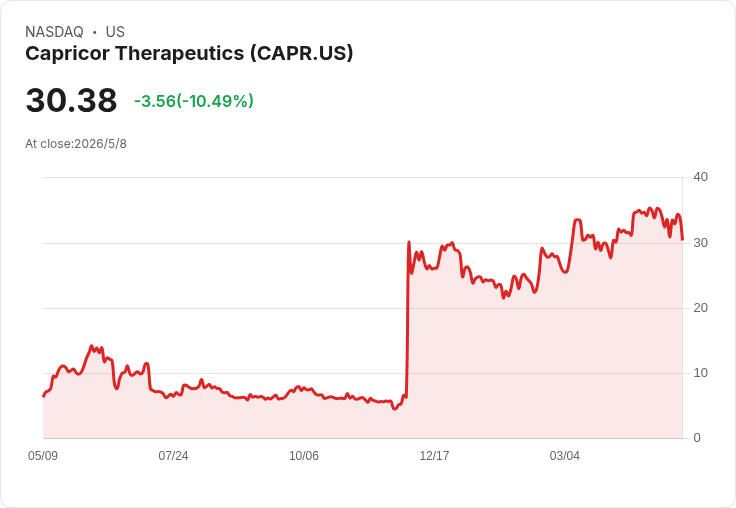
Capricor Therapeutics週五股價下跌約11%,原因是該公司在週四收盤後對日本藥廠Nippon Shinyaku提起訴訟,指控雙方2022年1月簽訂的美國分銷與商業化協議存在「基本定價缺陷」,並要求法院撤銷該協議及授權其直接或透過他方分銷Deramiocel(CAP-1002)。
背景與爭點: - 2022年1月的協議賦予Nippon Shinyaku在美國獨家商業化與分銷Deramiocel(CAP-1002),該藥為針對杜氏肌萎縮症(Duchenne muscular dystrophy, DMD)之候選療法。 - Capricor在宣告中指稱Nippon「未能充分為美國市場的商業上市做準備,並在其他方面實質違反美國分銷協議條款」,因此尋求撤銷協議、宣告其可自行或另尋分銷商分銷權、以及臨時禁制令等衡平救濟。 - 法規程序方面,Deramiocel於2025年7月收到美國食品藥物管理局(FDA)的Complete Response Letter(CRL),公司已回應相關疑慮,現行新的行動日期(PDUFA)為2026年8月22日。Capricor在2025年第四季財報電話會議中表示,若獲核准,Deramiocel有望成為首款同時改善DMD骨骼與心臟病變的療法。公司亦披露有約3.18億美元現金,為商業化提供部分資金後盾。
事實、影響與分析: - 市場反應迅速:訴訟公告發出後,市場對公司商業化能力與合作關係的信心受挫,短線拋售造成股價顯著回落。 - 若法院同意撤銷協議,Capricor可立即尋求直接分銷或另簽合作夥伴,理論上可加速商業化佈局;惟訴訟本身將增加不確定性、可能拖延上市準備且耗費資源。 - 即便FDA在2026年8月22日作出正面裁決,實際上市仍依賴有組織的商業準備(藥品供應、定價、保險給付與分銷網路)。Capricor主張Nippon在這些面向準備不足,但法院將以契約條款與證據判斷是否構成實質違約。 - 資金面來看,Capricor約3.18億美元現金提供短期運營及部分商業化準備的緩衝,但長期商業化與市場推廣仍需更多資源或夥伴協助。
替代觀點與回駁: - 反對觀點可能主張:CRL與FDA審查過程顯示主要障礙在法規而非Nippon的商業準備;或Nippon會以已盡合理努力為辯護。 - Capricor的回應與訴狀重點則在於合約所要求的商業準備義務是否已被履行,強調即使面臨法規不確定性,合作夥伴仍有責任為可能的上市情境完成商業化準備。最終裁決將取決於雙方在契約語句與實務執行上的具體證據。
結論與展望(行動號召): 此案將成為投資人與產業觀察者的關鍵觀察點:一方面關乎Deramiocel若獲核准時的商業化路徑與時程;另一方面也牽動生技公司與國際夥伴間的授權風險評估。建議投資人與利害關係人持續關注(1)法院後續訴訟進展與臨時禁制令申請結果、(2)Nippon Shinyaku的正式回應或反訴、以及(3)FDA在2026年8月22日的最終行動。這些事件將共同決定Deramiocel的商業前景與Capricor的未來策略。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
 免責宣言
免責宣言
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。

 發表
發表


 我的網誌
我的網誌